Page 51 - 2018食藥署年報(中文版)
P. 51
業者參考,亦於官網設立PIC/S GDP專區,公告政策與函示、通過名單、輔導計畫、
Q&A及教育訓練課程等資訊,作為業者執行時參考。
二、GDP實施時程及相關法規
本署於105年2月18日公告「西藥藥品優良製造規範(第三部):運銷」規範內
容及施行項目與時程,西藥製造業者及持有西藥許可證的販賣業者預計於108年起須
全面符合規定。為推動全面實施藥品GDP,衛福部積極完備法源,研擬藥事法第53-1
條及第92條修正草案,業於106年6月14日正式經總統令公布修正,並配合藥事法修
正,於106年12月28日發布西藥優良運銷準則,作為西藥販賣業者實施GDP之標準,
另於107年5月28日訂定發布「西藥運銷許可及證明文件核發管理辦法」作為後續申請
查核及核發許可等之管理需求,完備程序。
成果效益
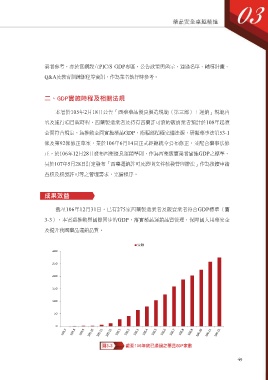
截至106年12月31日,已有275家西藥製造業者及販賣業者符合GDP標準(圖
3-3),本署藉推動與國際同步的GDP,落實藥品運銷品質管理,保障國人用藥安全
及提升我國藥品運銷品質。
家數
300
250
200
150
100
50
0
圖3-3 截至106年底已通過之藥品GDP家數
49