
2015 Annual Report
43
食品管
政策與
藥品管
管制藥
管理
醫療器
化粧品
國家實
檢驗
風險評
及科
國際合
兩岸
風險溝
消費
附
錄
5
隨著科技日新月異之發展、醫療保健科技化之需求,邁入老年化社會之危機,醫療
器材產業成為我國最具潛力的生技產業。面對國內醫療器材產業的活絡,本署強調以消費
者保護為核心,分別從法規管理國際化、生產源頭控管、上市前把關、上市後監督、藥商
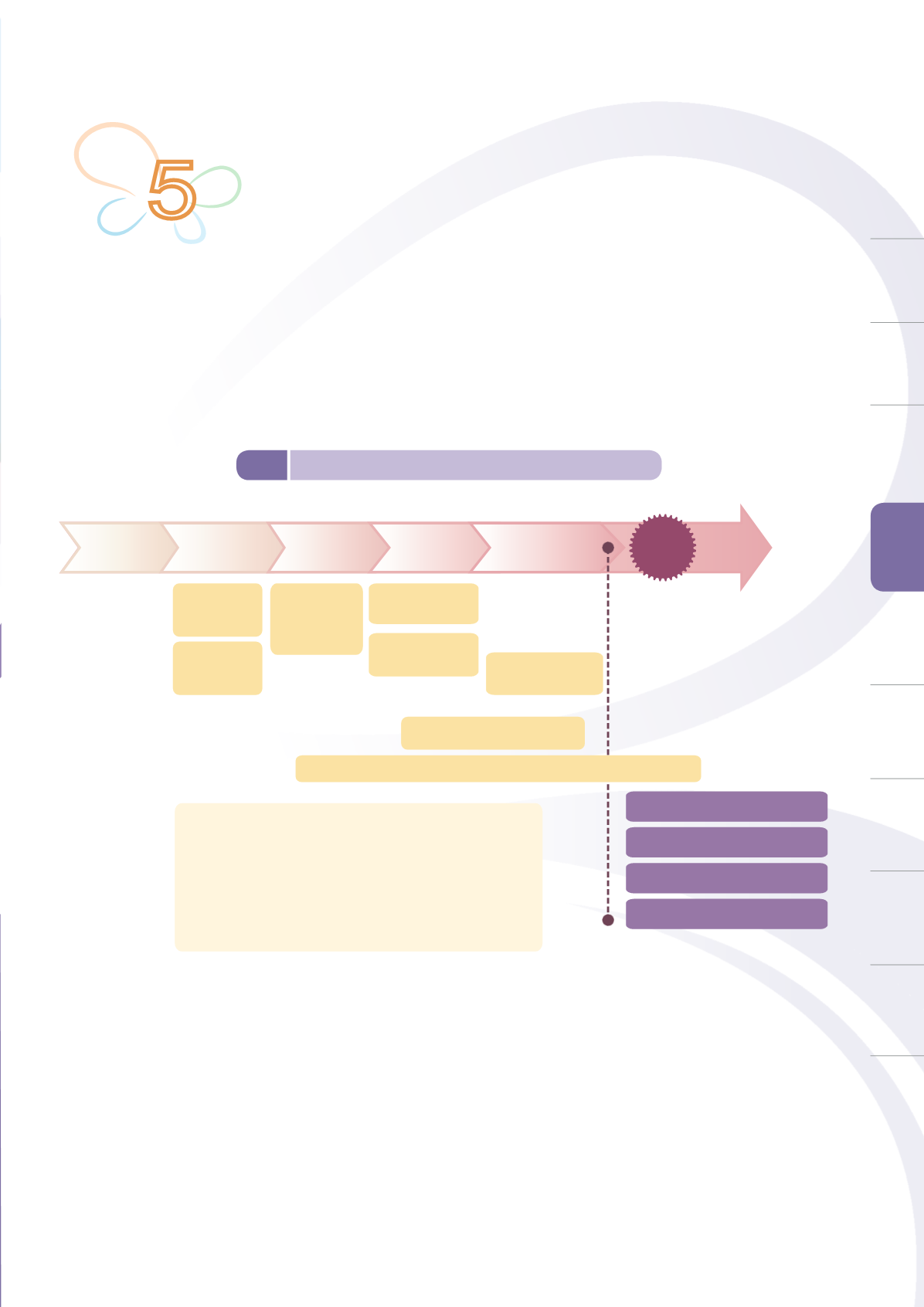
及產品通路管理及專業諮詢輔導,建立醫療器材全生命週期(
Total product life cycle
)品
質管理政策(圖
5-1
),有效控管醫療器材之安全、效能及品質,同時帶動我國生技醫藥
產業發展,共創消費者、業者及政府三贏之局面。
第一節 醫療器材法規標準及產品審查
現況
醫療器材為法規高度要求管理的產業,建立透明、有效率及合理的法規環境,使得以
保障國人使用安全及促進產業發展。為強化醫療器材產品上市前安全、效能品質之把關,
實施臨床前測試、臨床試驗及產品檢驗標準等查驗登記之管理項目審查。另針對我國創新
研發之申請案件,提供業者法規諮詢服務及專案輔導,是協助產業發展的重要利基。
醫療照護需求
基礎研究
一般/專案
諮詢輔導
醫材查驗登記檢
測實驗室規範
臨床試驗查核
(
GCP
)
查驗登記
(
Approval
/
Listing
)
臨床試驗計畫審
查
(
TFDA/IRB
)
產品屬性判定
生產源頭管理
產品設計
原型開發
臨床前
驗證
臨床試驗 上市申請
量產
上市
上市前把關
上市後監控
醫療器材專家委員諮議
製造廠品質系統稽查
(
GMP
)
安全監視及警訊蒐集
(
GVP
)
不良品/不良事件
通
報
(
ADR
)
消費者衛教宣導
優良流通規範
(
GDP
)
GLP
GTP
GCP
IRB
GMP
ADR
GVP
GDP
:
Good Laboratory Practice
(
實驗室優良操作規範
)
:
Good Tissue Practice
(
人體細胞組織優良操作規範
)
:
Good Clinical Practice
(
優良臨床試驗基準
)
:
Institutional Review Board
(
人體試驗委員會
)
:
Good Manufacturing Practice
(
優良製造規範
)
:
Adverse Drug/Device Reactions
(
藥物不良反應
)
:
Good Vigilance Practice
(
優良安全監控規範
)
:
Good Distribution Practice
(
優良流通規範
)
(
GLP/GTP
)
醫療器材管理
圖
5-1
我國醫療器材全生命週期管理體系



















