
食品管
政策與
藥品管
管制藥
管理
醫療器
化粧品
國家實
檢驗
風險評
及科
國際合
兩岸
風險溝
消費
附
錄
2015 Annual Report
33
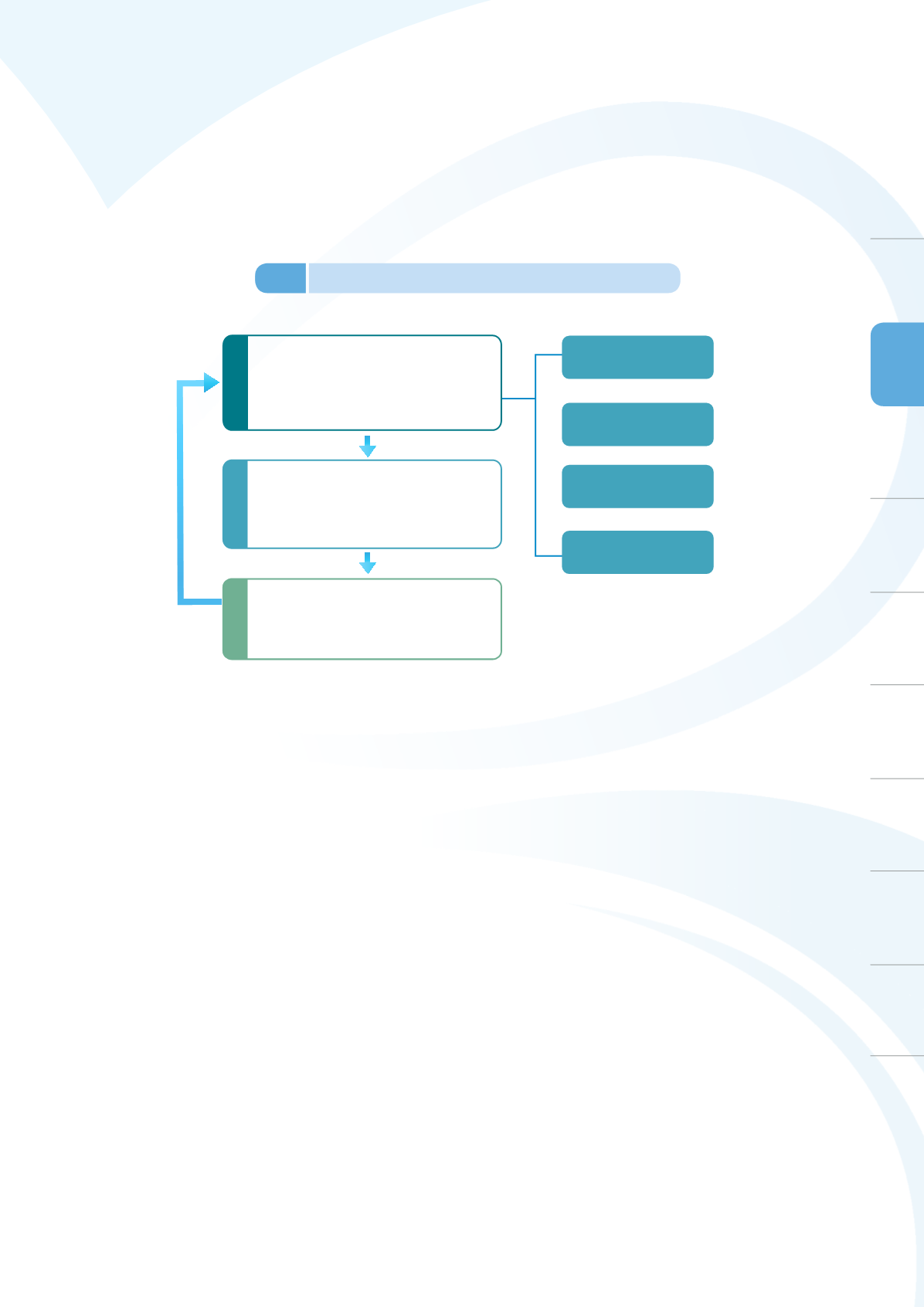
找出問題
分析問題
解決問題
安全性監控
安全性分析及評估
風險控制
以科學方法來釐清藥品之潛在安全性問
題,評估藥品之臨床效益及風險
( signal refinement )
針對藥品安全性問題,採取適當之風險管
控措施
(
如修改仿單、限縮使用、下市...
)
找出藥品使用潛在的安全性問題,
例如目前最常使用之自發性通報系統
( spontaneous reporting system)
不良反應通報系統
藥品監視期間定期
安全性報告
藥品安全主動監控機制
國內外安全警訊監控
(二)新藥安全監視
我國於
93
年公告「藥物安全監視管理辦法」,要求「新藥」核准上市初期,皆訂有「藥
品安全監視期間」,藥品許可證持有藥商須積極收集藥品上市後之所有安全性資料,定
期交付「藥品定期安全性報告」。至
103
年底,監視中藥品共計
291
項。
(三)國內外藥品安全警訊監控
每日監控國內外藥品安全警訊,必要時先行發布警訊,以提醒醫療人員及民眾注意用藥
安全,並進行藥品安全再評估作業。
103
年共計監控國內外藥品安全警訊共計
167
則。
(四)藥品安全主動監控機制
自
99
年起逐步建立以本土資料庫為主之藥品安全主動監控機制,針對高風險藥品,運
用健保資料,主動監控瞭解藥品於國內實際使用安全情形,以供藥品安全再評估或擬
訂風險管控措施之參考。
二、藥品安全再評估及風險管控
針對所監測具安全疑慮藥品,彙整國內外相關資料,進行藥品安全性再評估,必要時
採取風險管控措施。
103
年共計進行
59
項藥品安全性再評估,其中
22
項藥品採取風險管控措
施,包括
21
項藥品要求修改仿單或限縮使用,另外針對含
Chloramphenicol
或
ketoconazole
口
服製劑藥品經評估其風險大於臨床效益,要求該藥品下市。
圖
3-8
藥品上市後安全管控流程



















